肠道健康资讯
Microbiome:碳水、蛋白质、脂肪进入肠道后,它们发生了什么?
2019-10-18 02:00 来源:新营养
中国有句俗语说“病从口入”,指出身体疾病与人类饮食习惯、饮食结构有着密切的关系。不少人认为,吃了有毒有害的食物,身体才会生病,其实不然,当体内三大营养物质处于不均衡时,就会会滋生许多慢性疾病,例如糖尿病、高血压、高血脂等。
不论你爱吃肉还是吃素,都在为身体供给糖类、脂肪、蛋白质这三大营养成分,补充能量,支持正常的生命活动。那么它们到底是如何作用的呢?许多文献就三大营养成分进行了深入研究,研究人员称,营养物质需要在消化系统内需经一系列消化酶的分解,从复杂的大分子变为比较简单的有机物,才能被小肠所吸收。在这个过程中,肠道微生态扮演着重要的角色,它可以帮助分解复杂结构的分子,让营养素直通胃肠道,同时产生了大量的微生物代谢产物,被身体局部和全身吸收到血液中所用。
由于肠道菌群具有强大的代谢能力,会分解出种类繁多的代谢产物,因此对人体健康有积极的影响。圭尔夫大学在Microbiome发表的一篇重要综述, “Macronutrient metabolism by the human gut microbiome: major fermentation by-products and their impact on host health”,详细总结了肠道菌群如何分解三大营养物质(碳水化合物、蛋白质和脂肪),通过研究关键的微生物种类和相关的疾病状态,来全面理解微生物代谢产物对宿主健康的作用。

图源:Microbiome 官网
肠道微生态和三大营养素
人类肠道微生物群落是一个复杂的微生物生态系统,它位居肠道之内并且维持着肠道的动态平衡。肠道微生物是系统中功能贡献最大的相对遗传因子,总的来说,微生物可以将宿主营养物质的外源性和内源性底物进行代谢,会发酵众多微生物代谢产物,从而影响宿主的整体健康。碳水化合物、脂肪、蛋白质作为人体正常新陈代谢的基础物质,在生物体内的代谢是同时进行的,它们之间既相互联系,又相互制约。目前关于肠道微生物与三大营养成分代谢的研究,主要涉及的代谢产物包括短链脂肪酸和醇(主要产生单糖)、氨、支链脂肪酸、胺、硫化合物、酚和吲哚(主要产生氨基酸)、甘油和胆碱衍生物(从脂质分解)以及二氧化碳和氢等。
肠道微生物的初步代谢
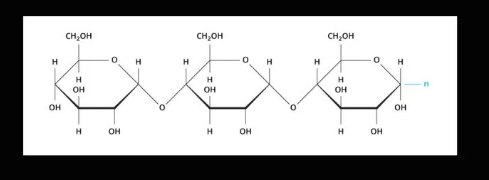
图示:碳水化合物分子结构
说到碳水化合物,分子架构由碳、氢、氧构成,可以简单理解为糖。作为身体主要的供能物质,它占人体所需能量的50~70%。日常食物中的糖以淀粉、多糖和双糖为主。其中单糖可以直接被人体消化,而多糖由于是多种单糖各种键组成连接,因此需要通过微生物中酶的催化水解成单糖才能被吸收。
食物中的淀粉转化,需要经唾液酶催化淀粉中α-1,4-糖苷键的水解,初步形成葡萄糖、麦芽糖、麦芽寡糖及糊精等产物。之后通过肠道当中微生物碳水化合物酶的作用,最后在小肠部位消化。例如拟杆菌基因中具有260种糖苷水解酶,主要分解淀粉和纤维素类。
此外,饮食中的蛋白质也需要水解成氨基酸及小分子肽后才能被吸收。由于唾液中不含水解蛋白质的酶,因此对蛋白质的消化从胃开始,肠道细菌可产生天冬氨酸、半胱氨酸、丝氨酸和金属蛋白酶,主要部位在小肠。在正常情况下,人和动物体所需要的能量主要由糖类氧化供给,但当糖类出现代谢障碍,供能不足时,则由脂肪和蛋白质氧化供给能量,保证机体的能量需要。由于蛋白质在人体当中比其他物质需要更多的步骤进行转化,因此对于肠道微生物来说,通过发酵氨基酸产生能量的情况较少。
丙酮酸代谢
身体微生物中在糖代谢中会分解出具有关键作用的中间产物丙酮酸,由α-酮酸糖代谢酵解,并且通过琥珀酸、乳酸或乙酰辅酶A循环,实现体内糖、脂肪和氨基酸间的互相转化。丙酮酸经过进一步的分解可以成为短链脂肪酸(SCFAs),如乙酸盐、丙酸盐和丁酸盐被宿主利用供能,因此丙酮酸在粪便样本中浓度并不高。
SCFAs在人体内参与不同的代谢,在线粒体内进行β-氧化提供能量,约占人体所需能量的5%~15%,占正常结肠上皮细胞所需能量的60%~70%。其中乙酸是宿主细胞能量的重要来源, 约提供人体总能量的10%;丙酸通过血液循环进入肝脏,在肝脏中分解代谢,参与丙酮酸逆转化为葡萄糖的过程;丁酸是上皮细胞的主要能量来源,还可以提高结肠上皮细胞的完整性。因此,SCFAs主要参与肠道能量供应,并且会影响肠腔pH、肠黏膜屏障的通透性,还可发挥调节免疫及抗肿瘤作用。
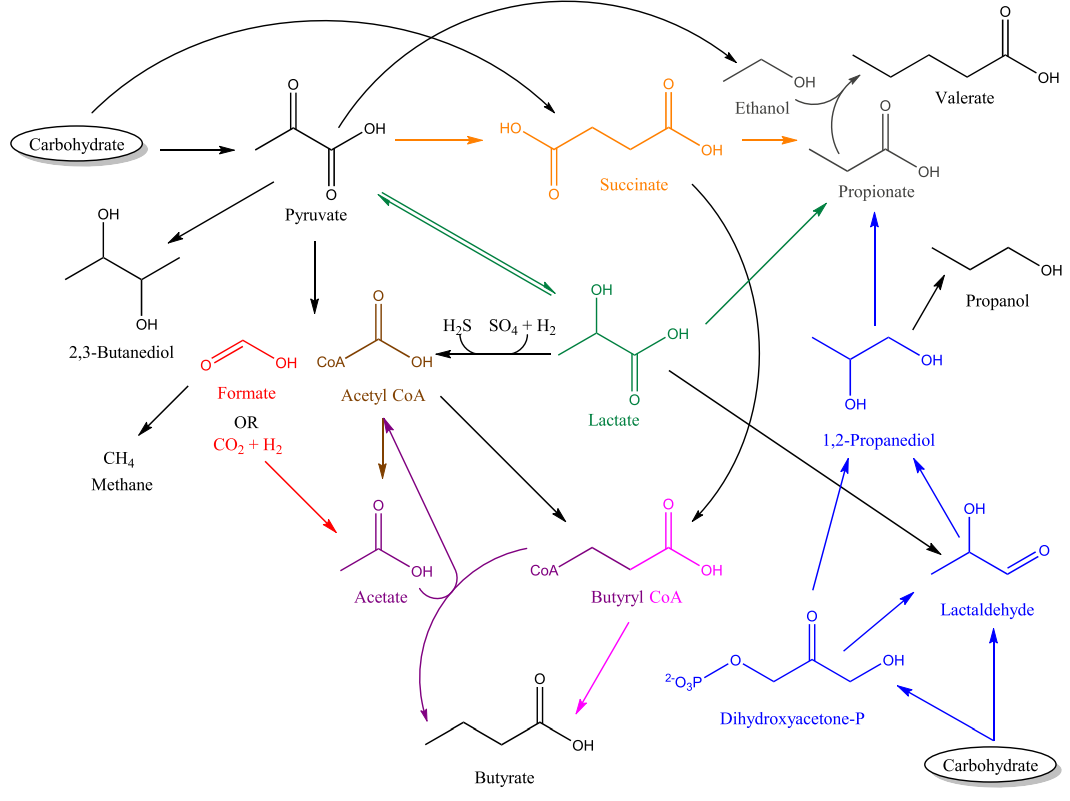
图示:人肠道微生物群分解代谢丙酮酸的策略 碳水化合物会首先分解为丙酮酸,并且转化为琥珀酸、乳酸、乙酰辅酶A,最终的发酵产物(乙醇、丙醇和2,3-丁二醇)。其中乙酸盐有两条途径:直接转化乙酰辅酶A产生能量(棕色)或乙酸化(红色);丙酸盐有三条途径:琥珀酸通路(橙色),丙烯酸酯通路(绿色)或1,2-丁二醇通路(蓝色);另外丙酸可以与乙醇联合发酵成为戊酸酯(灰色);丁酸盐由两个途径:丁酸激酶途径(粉红色),丁酰基辅酶A、乙酰辅酶A乙酰基转移酶通路(紫色)。
丙酮酸通过果胶降解、内源性细胞蛋白去甲基化调节或与维生素B12合成的醇会被运送至肝脏,帮助肝脏解毒之外,还能调节内源性醇的浓度来控制非酒精性脂肪肝(NAFLD)的发展。此外,变形菌门特别具有产生醇的能力,与炎症性肠病(IBD)中的失调呈正相关。
肠道气体代谢的核心是氢气
肠道内最常见的气体有5种,氮气、氧气、二氧化碳、氢气和甲烷。体内关于氢气的利用有多种,例如被动物细胞代谢利用、通过皮肤释放等。它是肠道细菌消化碳水化合物的常见代谢产物,细菌制造氢气是经过糖酵解途径,具体有三种:(1)乙酸菌乙酰化,例如Blautia spp,可将二氧化碳和氢转化为乙酸酯;(2)甲烷菌甲烷化,Methanobrevibacter可将二氧化碳和氢转化为甲烷;(3)硫还原菌,Desulfovibrio将硫酸盐加氢转化为硫化氢。虽然这些细菌利用氢气能量转化效率不同,但是这些细菌都共同生长在人类肠道内。
其中硫酸盐还原菌是最有效的氢营养菌,是一类以硫酸盐为呼吸链终端电子受体,从而氧化有机物和氢气以获取能量的一类厌氧微生物。硫酸盐还原菌代谢过程的副产物会出现硫化氢,它具有细胞毒性和遗传毒性,能腐蚀肠黏膜,并且会让屁具有臭鸡蛋气味。
氨基酸的分解代谢
蛋白质是结构复杂的有机大分子化合物,基本结构单位是氨基酸。不同来源的蛋白质(植物和动物)、食品加工方式、营养素比例、运输时间都会影响肠道微生物对于氨基酸的利用,其中氨基酸重要的代谢产物有短链脂肪酸、支链脂肪酸,同时在肠道微生物发酵过程中也会产生对健康有害的胺、酚类/吲哚和含硫化合物等,可能导致炎症、血管硬化、痴呆,甚至癌症的发生。
氨基酸分解代谢的主要途径是通过肠道微生物群进行脱氨基作用,所产生的氨,在正常情况下主要在肝脏合成尿素来排毒;只有少部分氨在肾脏以铵盐的形式由尿排出。虽然各种氨基酸在结构上具有共性,但不同的氨基酸由于结构的差异,也各有其特殊的代谢方式。例如亮氨酸、异亮氨酸和缬氨酸在开始阶段经转脱氨基作用生成各自相应的α-酸;然后再经过若干代谢步骤,缬氨酸分解生成琥珀酸辅酶A;亮氨酸和异亮氨酸生成乙酰辅酶A 及乙酰乙酰辅酶A。支链脂肪酸也是氨基酸代谢的重要部分,目前支链脂肪酸(BCFAs)对身体健康的影响还需要进一步的研究,初步研究表明BCFA能够像SCFAs一样调节肝脏中的糖和脂代谢。而含硫、碱性和芳香性氨基酸中在代谢过程中则会产生促炎、细胞毒性和神经活性化合物等负面效果。
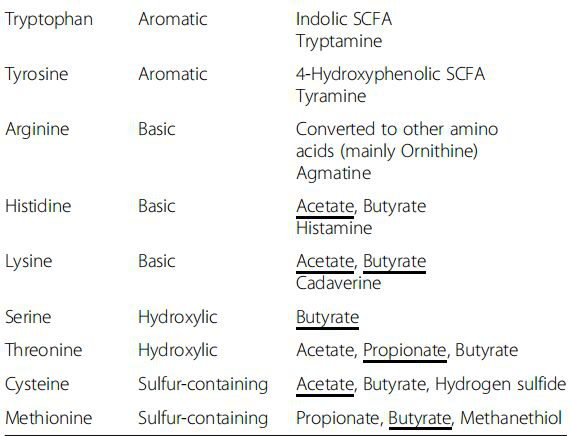
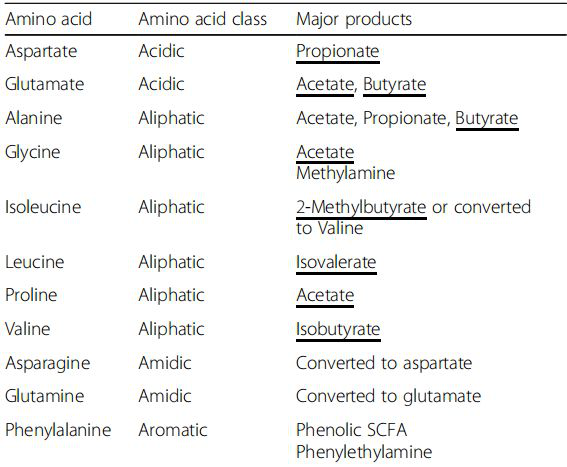
图示:存在于人类肠道微生物群及其代谢中的主要属及其代谢
基本的氨基酸代谢
天然的氨基酸现已经发现的有300多种,其中人体所需的氨基酸约有22种,分非必需氨基酸和必需氨基酸(人体无法自身合成)。氨基酸代谢共分三条途径:(1)合成各种组织蛋白,酶和激素;(2)通过氨基转换作用形成人体的非必需氨基酸;(3)通过脱氨基作用形成含氮部分和不含氮部分,其中含氮部分在肝脏中转化成尿素排出体外,不含氮部分又有两条代谢途径,一是氧化分解成二氧化碳和水,释放能量,二是转化成糖和脂肪。
肠道微生物群可以进行脱羧基作用菌种有很多,包括双歧杆菌、梭菌、乳酸菌、肠球菌、链球菌和肠杆菌等。例如精氨酸可以通过脱氨基作用生成胍基丁胺、腐胺、亚精胺和精胺等,胍基丁胺是一种调节多种神经递质和信号通路的神经调节剂,能够抑制一氧化氮合酶和减少其他多胺的合成,有效地缓解代谢综合征等疾病,但是过量的胍基丁胺水平对身体有负面影响。腐胺是亚精胺和精胺的前体,它可以在亚精胺合酶作用下转变成亚精胺,而后又转变成精胺。有研究提出,精胺和亚精胺能减轻氧化应激和通过自噬刺激延长细胞的寿命。
精氨酸另外可以转化为谷氨酸,可脱氨生成4-氨基(GABA),它是中枢神经系统的主要抑制性神经递质,其受体表达的变化与抑郁症和焦虑的发病机制密切相关。研究表示,酸杆菌和双歧杆菌可以让老鼠产生GABA,减轻皮质甾酮引起的压力和焦虑,减少抑郁行为。同时 GABA可以促进T细胞的增殖,帮助机体调节免疫力。
组氨酸在组氨酸脱羧酶的作用下可合成组胺,它是导致机体处于致敏状态的重要介质。广泛分布体内,外周组胺主要存在于肥大细胞内,而中枢神经系统组胺则由特定的神经细胞合成。目前已经证明组胺酸产生的组胺抑制了IL-1和IL-12产生促炎细胞因子,还会防止肠杆菌的易位。组胺也一种神经递质,可以调节身体疼痛知觉、学习记忆、树突细胞活性等。
赖氨酸的分解代谢可以产生尸胺,是尸臭的主要成分。尸胺的存在会给身体健康带来隐患,因为它们具有潜在的毒性,如果尸胺含量过大,则会让体内拥有高浓度的尸胺碱,容易患溃疡性结肠炎(UC)。
酪氨酸由肠球菌和肠杆菌分解代谢可以产生酪胺、苯丙醇和对香豆酯。医学界著名的“奶酪反应”就表现为,使用单胺氧化酶抑制剂治疗或食用含酪胺价高的食物,使得体内酪胺降解受阻而产生拟交感神经作用,表现为急性严重的高血压、恶心、心律失常、偏头痛等。酪胺广泛存在于各种各样的食物中,例如啤酒、牛奶、陈年奶酪、巧克力、腌制肉类、熏鱼等。因此,如果经常头痛的人们,要避免食用富含酪胺的食物。
苯酚和对甲酚是酚代谢物,其已被显示为降低肠上皮的完整性和IECS的生存力,并且可被许多肠道细菌物种(例如肠杆菌科成员和梭菌I、XI和XiVA)诱导产生。
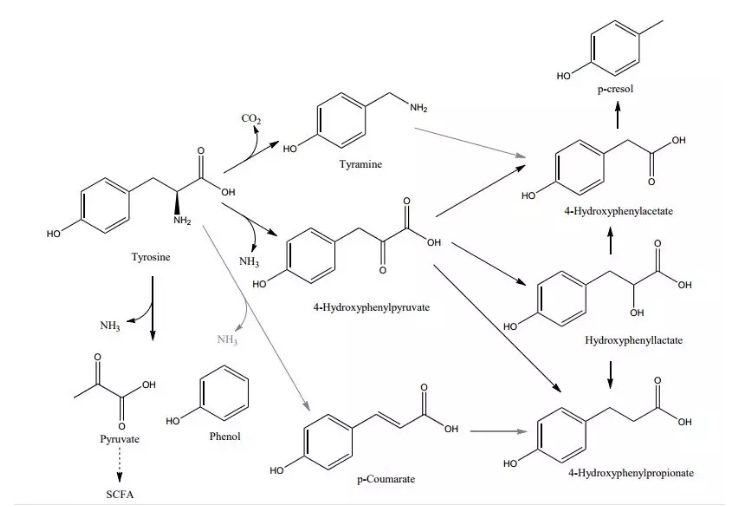
图示:酪胺酸的分解代谢
含硫氨基酸的代谢
由于蛋氨酸、半胱氨酸、牛磺酸、苯丙氨酸等必须氨基酸都含有硫元素,因此称为含硫氨基酸。它们通过肠道微生物分解代谢产生硫化氢和甲硫醇;其中硫化氢可以被甲基化为甲醇,甲醇可以进一步甲基化为二甲基硫醚,这种甲基化被也认为是解毒过程的一部分,随着代谢的深入化合物的毒性逐渐降低。然而,甲醇也可以转化为硫化氢,然后氧化成硫酸盐,进行解毒;这种硫酸盐可以被硫酸盐还原菌所利用。
蛋氨酸、半胱氨酸及胱氨酸三种含硫氨基酸的代谢是相互联系的,蛋氨酸可以转变为半胱氨酸和胱氨酸,半胱氨酸和胱氨酸也可以互变,但半胱氨酸及胱氨酸不能转变为蛋氨酸,所以半胱氨酸及胱氨酸是非必需氨基酸或条件必需氨基酸,而蛋氨酸则是必需氨基酸。
芳香氨基酸的代谢
芳香氨基酸包括苯丙氨酸、酪氨酸和色氨酸。苯丙氨酸在体内经苯丙氨酸羟化酶(phenylalanine hydroxylase)催化生成酪氨酸,然后再生成一系列代谢产物。苯丙氨酸羟化酶存在于肝脏,是一种混合功能氧化酶,该酶催化苯丙氨酸氧化生成酪氨酸,反应不可逆,因此酪氨酸不能还原生成苯丙氨酸,所以苯丙氨酸是必需氨基酸而酪氨酸是非必需氨基酸。体内的苯丙氨酸蓄积,可经转氨基作用生成苯丙酮酸,后者进一步转变成苯乙酸等衍生物,因此会导致尿液中有大量苯丙酮酸等代谢产物出现,严重者会产生苯丙酮尿症(phenyl ketonuria,PKU),这是一种先天性代谢性疾病。
与此同时,苯丙酮酸的堆积对中枢神经系统有害,会影响婴幼儿之后的智力发育,因此在对患儿疾病早期,应适当控制膳食苯丙氨酸含量。
苯丙氨酸的分解代谢能产生苯乙胺和反式肉桂酸。与酪氨酸和色氨酸不同,人们对苯丙氨酸衍生代谢物知之甚少。苯乙胺是一种神经递质,其作用是脱羧产生的内源性安非他明,通过促进儿茶酚胺和5-羟色胺的释放,可提高了情绪、精力和注意力。摄入苯乙胺也会使转换成苯乙酸酯,引起个体头痛、头晕等不适,意味着过量摄入会产生负面影响。研究发现,反式肉桂酸和对香豆酸与心血管疾病呈负相关。
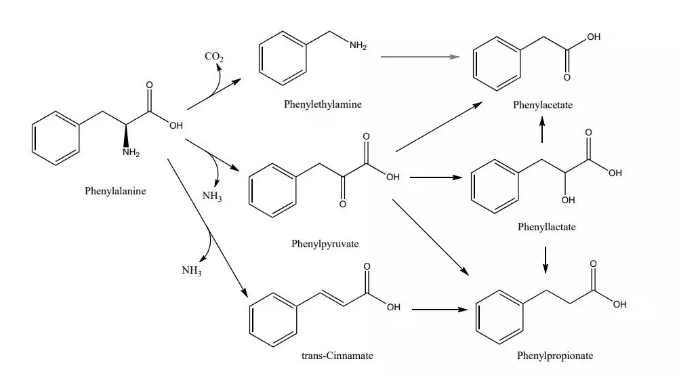
图示:苯丙氨酸的分解代谢
色氨酸的分解代谢可以产生色胺和吲哚。色胺是一种神经递质,在调节肠道运动和免疫功能中具有重要作用,尤其是它能与吲哚胺,2,3-双加氧酶和芳基烃受体相互作用,可以加强身体免疫监测,抑制促炎细胞因子的表达。此外,色胺与许多疾病包括炎症性肠病,肠易激综合症、心血管疾病、和骨质疏松症等相关。
吲哚是由许多种类的拟杆菌和肠杆菌科细菌分解色氨酸产生的主要代谢产物,会影响分子活性、生物膜形成、抗生素耐药性、体内毒性,抑制病原体的殖民能力等方面。它通过与孕烷受体和芳基烃受体相互作用,在宿主防御中起着重要作用。有证据表明,吲哚生产过剩会增加肝脏的负担,引发尿毒症毒素与慢性肾脏疾病等疾病。
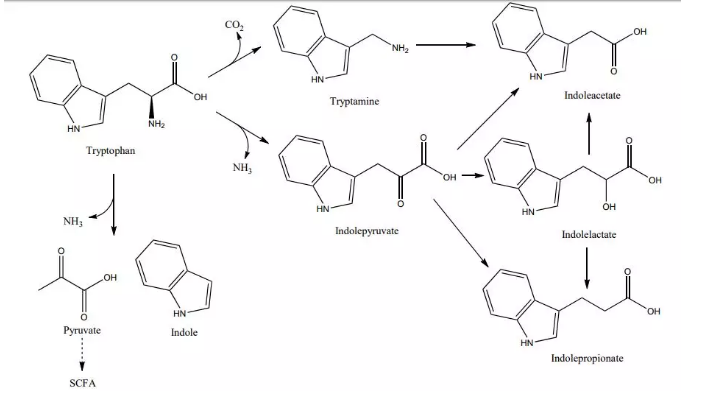
图示:色氨酸的分解代谢
脂质的分解代谢
脂质组成复杂,包括甘油三酯、胆固醇、磷脂、脂肪酸以及少量其他脂质。其中甘油三酯代表膳食脂肪总量的95%,而磷脂主要以磷脂酰胆碱的形式,占比虽然少,但却是细胞的主要组成部分。脂质会通过肠道内的某些细菌,包括乳酸菌、肠球菌、梭菌和变形菌等,将甘油还原为1,3-丙二醇。3-羟基丙醛(3-羟脯氨酸)是这一过程的中间产物,已被报道在乳杆菌和肠球菌培养物中以细胞外方式积累。
胆碱是生成卵磷脂的必须物质,还可以被肠道微生物群梭菌( Lactobacillus and Enterococcus spp)代谢成三甲胺,它在肝脏中被氧化成三甲胺氮氧化物,并且促进泡沫细胞(富含脂质的巨噬细胞)的产生而加剧动脉粥样硬化,导致高的胆固醇水平。因此高三甲胺氮氧化物水平会影响血清水平增高,容易导致动脉粥样硬化和心血管疾病的发生。但是目前关于肠道微生物群介导的脂质代谢与身体健康作用机制仍不明确,还需要进一步的研究。
影响内源性底物的利用率
研究发现,外源性底物代谢将大大影响内源性底物的肠道微生物群的使用,例如膳食纤维可以减少粘蛋白的降解,它是一种酸性糖蛋白,广泛覆盖在管状器官以及身体器官等上皮细胞表面。肠道微生物群的粘蛋白合成是一个自然发生的过程,并且受到不同外源性食物的影响。当体内粘蛋白水平较高时,会对身体起到负面作用。而且,膳食脂肪摄入也能改变胆汁酸的分布,胆汁酸是胆汁中的主要成分,是胆固醇经肝组织代谢的最终产物,它可以调节胆汁酸重吸收、炎症、控制甘油三酯,帮助人体促进肝脏内的脂肪代谢,避免沉积,并且分解肠道内毒素。
结论
肠道菌群对人体健康的作用正在被慢慢发掘,除了现今已知的肠脑轴,肠肝轴、肠肺轴、肠肾轴、肠肌轴都在不断打破人们的固有认知,为研究人员发掘疾病根源、寻找健康契机提供了新的方向。例如碳水化合物经过肠道代谢产生的SCFAs受到行业关注,关于SCFAs如何在到达肝脏时调节葡萄糖代谢和脂肪沉积,肠道微生态与蛋白质和脂肪降解还在研究当中。
由于代谢物的多样性和微生物途径的复杂性,通过微生物途径可以进一步了解肠道微生物生态系统循环,调节系统去除代谢所产生的有毒物质,让有益物质发挥积极作用,减少有害物质对健康的影响,从而维持微生物平衡,保持个体健康。
参考文献:
1.三大营养物质如何被肠道菌群代谢(综述)-热心肠日报
2.Macronutrient metabolism by the human gut microbiome: major fermentation by-products and their impact on host health | Microbiome | Full Text
3.Li J, Jia H, Cai X, Zhong H, Feng Q, Sunagawa S, et al. An integrated catalog of reference genes in the human gut microbiome. Nat Biotechnol. 2014;32:834–41.
4.Turnbaugh PJ, Ley RE, Hamady M, Fraser-Liggett C, Knight R, Gordon JI. The human microbiome project: exploring the microbial part of ourselves in a changing world. Nature. 2007;449:804–10.
5.Human Microbiome Project Consortium. Structure, function and diversity of the healthy human microbiome. Nature. 2012;486:207–14.
新营养留言互动
您的电话不会被公开。 必填项已用 * 标注
相关热词搜索:
新营养峰会/活动
新营养热门资讯
新营养周报 | 农夫山泉上新蓝靛果混合汁
数据 / 观察 · 01-06
新营养周报 | 蒙牛推出早餐奶新品、纽曼
数据 / 观察 · 12-29
一图读懂 | 2024新营养肠道微生态格局与
XINGRAPHIC · 12-29
新营养周报 | 达芬奇优形推出纤体杯新品
数据 / 观察 · 12-23